
 Стаття
Стаття
 21.02.2026
21.02.2026
Особливості вибору та застосування очних крапель з гіалуроновою кислотою при синдромі сухого ока
Сидорова М.В. Медичний центр «Добробут», м. Київ, Україна
Резюме. Органи зору є вкрай вразливими до зовнішніх факторів, а слізна плівка забезпечує взаємодію очного яблука із суміжним повітрям та виконує захисну, оптичну та трофічну функції. Порушення слізної плівки, зумовлені її нестійкістю або зниженням виробництва сліз, призводить до синдрому (хвороби) сухого ока. Гіперосмолярність слізної рідини стимулює каскад патофізіологічних реакцій і розглядається як основна причина запалення поверхневих структур ока. Базовою терапією синдрому сухого ока є зволоження очної поверхні. З обґрунтованим успіхом у клінічній практиці застосовуються краплі з гіалуроновою кислотою (ГК) — унікальною природною речовиною, мукополісахаридом з високою здатністю зв’язування з водою та великою в’язкістю. Об’ємна в’язкість розчинів гіалуронату сильно залежить як від концентрації, так і від молекулярної маси, двократне збільшення концентрації або молекулярної маси призводить до 10-кратного збільшення об’ємної в’язкості розчину. Унікальна в’язкопружна природа ГК разом з її біосумісністю та неімуногенністю, максимальна відповідність фізико-хімічним властивостям натуральної сльози сприяють покращенню стійкості слізної плівки та зменшенню вимивання ГК з очної поверхні між морганнями (висока об’ємна в’язкість) та водночас не утруднює безперервне моргання завдяки низькій зсувній в’язкості. У лікуванні синдрому сухого ока перевагу слід надавати очним краплям без консервантів, препаратом першого вибору в лінійці засобів для зволоження ока є 0,4% очні краплі ГК без консервантів. Використання очних крапель Гілайс® рекомендовано як для покращення комфорту очей при користуванні гаджетами, так і для лікування складних форм синдрому сухого ока. Препарат ефективно підвищує стабільність слізної плівки, забезпечує комфорт поверхні ока та захист від пересихання, формує гладеньку поверхню рогівки і є вибором при носінні контактних лінз. Гілайс® сприяє кращому загоєнню після травм, опіків, операцій та усуває прояви сухого ока.
Ключові слова: слізна плівка, синдром сухого ока, сльозозамісна терапія, гіалуронова кислота.
Зоровий аналізатор є надзвичайно важливим компонентом системи органів чуття для сприйняття людиною інформації про зовнішній світ. Водночас органи зору є вкрай вразливими як до факторів зовнішнього середовища, так і до ендогенних порушень. Слізна плівка — це складний динамічний функціональний комплекс, що забезпечує взаємодію очного яблука з суміжним повітрям та виконує низку функцій. Захисна функція слізної плівки полягає у запобіганні висиханню рогівки та її ураженням дрібними сторонніми предметами, видаленні часточок пилу, бактерицидній дії. Оптична функція заломлення світлових променів забезпечується шляхом згладжування нерівностей поверхні рогівки та підтримування її вологості, гладкості та дзеркальності. Трофічна функція передбачає участь у процесах дихання та метаболізму рогівки. Також слізна плівка є змазкою для рухливості повік. Порушення слізної плівки, зумовлені її нестійкістю або зниженням виробництва сліз, асоціюються з дискомфортом в очах і/або візуальними симптомами та запаленням структур поверхні ока. Таке порушення призводить до синдрому (хвороби) сухого ока. Експерти Міжнародної робочої групи з сухого ока (Dry Eye Workshop, DEWS) та Товариства слізної плівки і поверхні ока (Tear Film and Ocular Surface Society, TFOS) дійшли висновку, що механізмами розвитку синдрому сухого ока є недостатність продукції слізної рідини та/або надмірна її втрата через випаровування. Найбільш поширеним механізмом сухості ока є надмірне випаровування, далі йдуть комбіновані порушення, ізольована недостатність слізної рідини є найменш поширеним станом [1].
Традиційно синдром сухого ока характеризується втратою об’єму сліз, водним дефіцитом, раннім розривом слізної плівки, що призводить до гіперосмолярного пошкодження тканин очної поверхні. Унаслідок цього виникає запалення, втрата як епітелію рогівки, так і келихоподібних клітин кон’юнктиви. Подальше зменшення зволоження очної поверхні призводить до більш швидкого розриву слізної плівки, посилює гіперосмолярність сліз і замикає порочне коло патогенезу [2].
Гіперосмолярність слізної рідини розглядається як основна причина запалення поверхневих структур ока, тому що вона стимулює каскад патофізіологічних реакцій у поверхневих епітеліальних клітинах через мітогенактивовану протеїнкіназу та прозапальні цитокіни (інтерлейкін 1а та 1b, фактор некрозу пухлини). Унаслідок запалення відбувається апоптоз епітеліальних клітин рогівки та келихоподібних клітин кон’юнктиви [3].
Протягом більше ніж півстоліття будову слізної плівки розглядають як тришарову модель, запропоновану E. Wolff у 1946 році. Згідно з цією моделлю шар муцину, що покриває очну поверхню, знижує передбачувану гідрофобність епітеліальних клітин. Водний шар відповідає за змазування, деякі поживні речовини, антимікробні білки та оптимальну осмолярність для захисту оголеного очного епітелію. Ліпідний шар запобігає втраті водного шару через переливання та випаровування. Згідно із сучасною двошаровою моделлю будови слізної плівки прийнято вважати, що водний та муциновий шари являють собою один шар водно-муцинового гелю, що становить основну частину тонкої (2–6 мкм) слізної плівки та частково інтегрований з поверхнею ліпідного шару. Ліпідний шар слізної плівки дуже тонкий, його товщина становить від 15 до 157 нм, із середнім значенням 42 нм. Він зменшує поверхневий натяг на повітряній межі слізної плівки рогівки і сприяє поширенню слізної плівки по очній поверхні. Склад ліпідного шару слізної плівки до кінця не вивчений, але, швидше за все, він має молекули поверхнево-активної речовини з боку слизової оболонки та ліпофільні молекули з боку повітря. Ліпідний шар відіграє важливу роль у стабілізації слізної плівки й у зменшенні випаровування сліз. Шари слізної плівки знаходяться у постійній динамічній взаємодії [4].
Хімічна структура слізної плівки дуже складна. За допомогою сучасних методів протеоміки у складі слізної плівки ідентифіковано понад 1500 білків та понад 200 пептидів, що походять з кількох із цих білків. Ліпідний профіль слізної рідини подібний до ліпідного складу секрету мейбомієвих залоз, але з порівняно більшим умістом фосфоліпідів. У слізній плівці містяться кисень, метаболіти та електроліти, антимікробні пептиди, білки та розчинні імуноглобуліни, які захищають очну поверхню від інфекції. На апікальних поверхнях епітелію рогівки та кон’юнктиви є трансмембранні муцини, які збільшують коефіцієнт зчеплення з водою, полегшуючи поширення сліз по очній поверхні. Трансмембранні муцини, прикріплені до епітеліальних мікроклітин, простягаються до 500 нм (0,5 мкм) у слізну плівку і також становлять лінію захисту епітеліальних клітин від інфекції та травм [4].
Причини порушення структури і функції слізної плівки численні. Це подовжений час перебування перед екраном (відеомонітори, телевізори, смартфони тощо), випромінювання, травми, кераторефракційні або з приводу катаракти хірургічні втручання, куріння, кондиціонування повітря, застосування діуретиків, антигістамінних препаратів, антидепресантів і протизапальних засобів тощо. У формуванні сухості ока також відіграє роль велика кількість ендогенних чинників. Це старший вік, жіноча стать, системні запальні захворювання (такі як ревматоїдний артрит, системний червоний вовчак, склеродермія), синдром Шегрена, розацеа, саркоїдоз, кератити [1].
Лікування синдрому сухого ока передбачає цілу низку заходів та медикаментозних засобів, серед них зволоження ока є базовою терапією цього стану. Існують різноманітні препарати для сльозозамісної терапії. Доведено, що сучасні препарати, що заміщують слізну рідину, мають порівняно однакову ефективність [1, 5].
Однією з основних проблем, пов’язаних із використанням звичайних офтальмологічних препаратів для місцевого застосування, є короткий час утримання компонентів на очній поверхні. Після закапування відбувається витікання лікарського засобу головним чином через моргання та сльозотечу, що знижує ефективність терапії. Це обумовлює потребу у частих інстиляціях для підтримання терапевтичної концентрації ліків у слізній плівці, що може погіршити прихильність пацієнта до лікування та призвести до очних та системних побічних ефектів. Уведення мукоадгезивних полімерів є однією з найбільш часто використовуваних стратегій продовження часу контакту препарату з епітелієм рогівки/кон’юнктиви. Додавання макромолекул збільшує в’язкість препарату, отже, швидкість елімінації крапель із передрогівкової ділянки зменшується. Більше того, мукоадгезивні макромолекули здатні тісно взаємодіяти з муциновим шаром, покриваючи рогівку та кон’юнктивальну поверхню ока [6].
З обґрунтованим успіхом у клінічній практиці для лікування синдрому сухого ока широко застосовуються краплі з гіалуроновою кислотою (ГК) — унікальною природною речовиною, однією з найцікавіших і найкорисніших природних макромолекул [7].
Гіалуронова кислота вперше була виділена зі склоподібного тіла бичачого ока, далі її виявили в культуральній рідині гемолітичного стрептококу. На сьогодні встановлено, що ГК притаманна всім живим організмам: вона міститься переважно у позаклітинному матриксі, незначна її кількість може існувати й внутрішньоклітинно. В організмі ГК зустрічається у формі солі, гіалуронату, і виявляється у високій концентрації в декількох м’яких сполучних тканинах, включаючи шкіру, пуповину, синовіальну рідину та склоподібне тіло. Значна кількість ГК знайдена також у легенях, нирках, мозку та м’язовій тканині [7].
За хімічною структурою ГК є мукополісахаридом, високополімерним несульфатованим глікозаміногліканом. Спочатку його виділили у вигляді кислоти, але у фізіологічних умовах він поводиться як сіль (гіалуронат натрію). Термін «гіалуронан» був уведений у 1986 році відповідно до міжнародної номенклатури полісахаридів та охоплює різні форми, які може прийняти молекула, наприклад кислотну форму, гіалуронову кислоту та солі, такі як гіалуронат натрію, що утворюються при фізіологічному рН [7].
Полімерна будова ГК являє собою лінійний (нерозгалужений) ланцюг із повторюваних дисахаридних компонентів: N-ацетил-β-D-глюкозаміну і β-D-глюкуронової кислоти. ГК не утворює ізомерів і завжди є хімічно ідентичною незалежно від способу та джерела отримання. Ця відносно проста структура зберігається однаковою в усіх ссавців, що має велике значення в біології [7]. Обидва цукри дисахариду просторово пов’язані з глюкозою, яка в бета-конфігурації дозволяє всім її об’ємним групам (гідроксилам, карбоксилатній частині та аномерному вуглецю на сусідньому цукрі) знаходитися в стерично сприятливих екваторіальних положеннях, тоді як всі малі атоми водню займають менш стерично вигідні осьові положення. Таким чином, структура дисахариду енергетично дуже стійка. Кількість повторюваних дисахаридних комплексів в одній завершеній молекулі гіалуронану може досягати 10 000 і більше, молекулярна маса ~ 4 млн дальтон (кожен дисахарид має масу ~ 400 дальтон). Середня довжина дисахариду становить ~ 1 нм. Отже, молекула гіалуронану з 10 000 повторів може розтягнутись на 10 мкм, якщо розтягнути її з кінця в кінець, довжиною, приблизно рівною діаметру еритроцита людини [7]. Довжина ланцюга гіалуронану визначає його як фізичні, так і фізіологічні властивості [8].
ГК притаманна висока здатність зв’язування з водою, що обумовлює її високу в’язкість. Гіалуронова кислота є однією з найбільш гідрофільних (водолюбних) молекул у природі, і її можна описати як зволожувач природи [7]. У фізіологічному розчині кістяк молекули гіалурону зміцнюється поєднанням хімічної структури дисахариду, внутрішніх водневих зв’язків та взаємодії з розчинником. Осьові атоми водню утворюють неполярну, відносно гідрофобну грань, тоді як екваторіальні бічні ланцюги утворюють більш полярну, гідрофільну грань, створюючи тим самим структуру звивистої стрічки, багатонитчастих пласких або надспіралізованих структур. Розчини гіалуронану виявляють дуже незвичні реологічні властивості: надзвичайно мастильні та дуже гідрофільні. Ці ланцюги заплітаються між собою при дуже низьких концентраціях, що обумовлює вказані реологічні властивості. У розчині полімерний ланцюг гіалуронану набуває форми випадковим чином збудованої сітки, яка затримує приблизно в 1000 разів більше води, ніж її власна вага. Ці унікальні якості ГК роблять розчини гіалуронану ідеальними лубрикантами [7].
Розчини ГК можуть бути високов’язкими, з властивостями неньютонівської рідини. При певній номінальній точці настає стан «перекриття сітки», коли ланцюги полімеру заповнюють розчин таким чином, що змушені торкатися один одного, хоча можуть взаємопроникати і при більш високих концентраціях. Експериментально встановлено точку «перекриття сітки», при збільшенні концентрації вище якої питома в’язкість починає різко зростати. Ця точка залежить одночасно від концентрації та молекулярної маси ГК. Для ГК з молекулярною масою 1 млн дальтон концентрація «перекриття сітки» становить приблизно 1400 мкг/см3 . Для ГК з молекулярною масою 6 мільйонів для перекриття потрібна концентрація лише близько 320 мкг/см3 [9].
Графічна характеристика реологічних властивостей розчинів гіалуронату як функції концентрації та молекулярної маси надана в роботах H. Bothner та Wolfgang G.K. Müller-Lierheim (рис. 1) [8, 10].
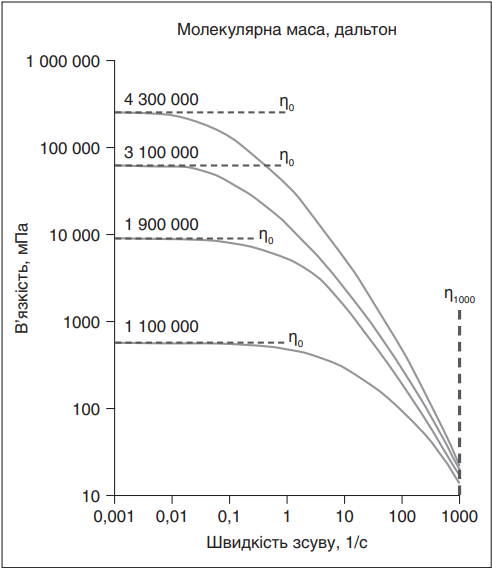
Об’ємна в’язкість розчинів гіалуронату сильно залежить як від концентрації, так і від молекулярної маси. Двократне збільшення концентрації або молекулярної маси призводить до 10-кратного збільшення об’ємної в’язкості розчину. Причому у розбавленій ділянці (низька концентрація гіалуронану) подвоєння молекулярної маси призводить до збільшення в’язкості в 1,67 раза, а в напіврозведеній ділянці (середня або висока концентрація гіалуронану) це призводить до збільшення в’язкості в 12 разів. Чим довшими є ланцюги гіалуронану, тим більше вони можуть сплутуватися і тим більше в’язкопружним є розчин [8, 10]. І мукоадгезивність, і в’язкість препаратів в основному залежать від молекулярної маси та концентрації полімеру. Є повідомлення, що остаточна в’язкість не повинна перевищувати 30 мПа, в іншому випадку може виникати дискомфорт через затуманений зір та відчуття стороннього предмета, що призводить до більш швидкої елімінації препарату через рефлекторну сльозотечу та моргання [6].
Біологічні функції ГК включають підтримку еластичності та пружності рідких сполучних тканин, таких як суглобова синовіальна та склоподібна рідина очей, контроль гідратації тканин та транспортування води, надмолекулярне складання протеогліканів у позаклітинному матриксі та численні рецепторні функції при відшаруванні клітин, мітозі, міграції, розвитку пухлини та метастазуванні й запаленні. Її функція в організмі, серед іншого, полягає у зв’язуванні води та змащуванні рухомих частин тіла, таких як суглоби та м’язи. Унікальна в’язкопружна природа ГК разом з її біосумісністю та неімуногенністю, здатність до біологічного розкладання дозволяють застосовувати її при цілій низці патологічних станів. Максимальна відповідність фізико-хімічним властивостям натуральної сльози сприяє успішному використанню розчинів ГК в офтальмології [7].
У контексті лікування синдрому сухого ока очні краплі з ГК довели свою ефективність як високобіосумісний замінник водної фази людських сліз. Завдяки унікальним реологічним властивостям застосування розчину ГК покращує стійкість слізної плівки та зменшує вимивання ГК з очної поверхні між морганнями (висока об’ємна в’язкість) та водночас не утруднює безперервне моргання завдяки низькій зсувній в’язкості. Зв’язування води та протидія зневодненню сприяють загоєнню епітеліальної рани. Результати клінічних досліджень із застосування ГК при лікуванні синдрому сухого ока свідчать про те, що розчини ГК є більш ефективними порівняно з фізіологічним розчином. Ефективність препаратів ГК у лікуванні сухого ока за деякими параметрами не поступається циклоспорину у покращенні об’єктивних ознак та суб’єктивних симптомів сухості очей [11–13].
Висока якість ГК залежить від молекулярної маси, яка пов’язана з довжиною ланцюга кожної молекули. ГК з високою молекулярною масою є більш згуртованою, оскільки для її руйнування потрібно більше часу, ніж для ГК нижчої молекулярної маси. Високомолекулярна ГК може більш тривало знаходитися на поверхні ока, щоб утримувати вологу, постійно зволожувати рогівку та сприяти регенеративному загоєнню. Низькомолекулярна ГК більш дисперсійна завдяки своїй невеликій вазі, може зв’язуватися з іншими молекулами та стимулювати запальну реакцію [14].
Очні краплі з високомолекулярною ГК виконують дві основні функції. Це утримання водного та секреторного муцину у водному шарі, що зменшує тертя між повіками та очною поверхнею, а отже, зменшує пошкодження та запалення очної поверхні. Стабільність слізної плівки посилюється завдяки зменшенню пошкодження очної поверхні та утриманню водного та секреторного муцину у водному шарі. Інша функція — протизапальний ефект, який може підтримувати секреторну експресію муцину Muc5AC. Цей ефект також підвищує стабільність слізної плівки. Таким чином, офтальмологічний розчин високомолекулярної ГК має вищий терапевтичний ефект, ніж низькомолекулярні препарати [15].
Як було вказано вище, з підвищенням концентрації ГК зростає в’язкість розчину і ефективність очних крапель у лікуванні. Ці дані були підтверджені на експериментальній моделі сухого ока, коли застосування 0,3% розчину ГК сприяло не тільки покращенню стабільності слізної плівки, але й збільшенню кількості келихоподібних клітин кон’юнктиви та зменшенню апоптозу клітин епітелію рогівки [2]. Серед препаратів ГК 0,3% розчини є більш клінічно ефективними, ніж 0,1% [11].
Також при виборі очних крапель слід мати на увазі осмолярність розчину. У той час як гіперосмолярність слізної плівки сприяє розвитку синдрому сухого ока, результати клінічних досліджень показали, що гіпотонічні розчини демонструють більшу ефективність порівняно з ізотонічними розчинами. Зменшуючи осмолярність слізної плівки, гіпотонічний розчин не тільки покращував її характеристики та життєздатність епітеліальних клітин рогівки та кон’юнктиви, але також виявився ефективним у зменшенні симптомів сухості очей [14].
У лікуванні синдрому сухого ока слід надавати перевагу очним краплям без консервантів, тому що останні можуть викликати алергічні реакції, є токсичними як для келихоподібних клітин кон’юнктиви, так і для слізної плівки через порушення ліпідного компонента [5].
Потреба у застосуванні сльозозамінників виникає вже при роботі з гаджетами. В основі «комп’ютерного синдрому» є порушення слізної плівки через зменшення частоти моргання, що призводить до більш значної втрати вологі та розриву слізної плівки. У таких ситуаціях може ще не відбуватися запального процесу, проте вже виникають показання для застосування замінників слізної рідини. При тривалому зоровому напруженні очні краплі з ГК створюють на поверхні ока захисну плівку, яка зволожує і живить око.
При розвитку запального процесу, суб’єктивних симптомів використання замінників слізної рідини стає невід’ємною частиною терапії. Згідно з рекомендаціями Buckinghamshire Healthcare NHS Trust Національної системи охорони здоров’я Великої Британії, препаратом першого вибору в лінійці препаратів для зволоження ока при синдромі сухого ока є 0,4% очні краплі ГК без консервантів [16].
Унікальним препаратом ГК на вітчизняному ринку є препарат Гілайс®, який відповідає основним вимогам для засобів лікування сухості ока. Це висока (0,4%) концентрація гіалуронату, висока молекулярна маса та відсутність консервантів. Стерильний офтальмологічний розчин випускається у флаконах по 10 мл, що є еквівалентом для більше ніж 250 крапель. Флакон оснащено інноваційним патентованим багатодозовим офтальмологічним дозатором натискного типу (OSD). OSD захищає розчин від потрапляння потенційно шкідливих бактерій, тому розчин залишається стерильним протягом 120 днів після першого використання.
До складу препарату Гілайс® входить офтальмологічний розчин гіалуронату натрію високої молекулярної маси, продукт біотехнологічного синтезу. Гіалуронат натрію має мукоміметичні, мукоадгезивні та в’язкопружні властивості, завдяки чому покращує стабільність слізної плівки та забезпечує комфорт поверхні ока — змащення, зволоження та захист. Зволожуючі та захисні властивості гіалуронату сприяють усуненню подразнення, відчуття сухості, печіння та стороннього предмета в очах через вплив навколишнього середовища, а саме вітру, сонця, сухого повітря, солоної води, диму, занадто яскравого світла, кондиціонованого повітря, опалення, тривалої роботи за комп’ютером, або у випадку хірургічної операції на очах, кон’юнктивіту чи частого або тривалого користування контактними лінзами. Препарат застосовують по 1 краплі в око 2–3 рази на добу та за потребою.
Таким чином, очні краплі з ГК без консервантів є безпечними у застосуванні. Вони не впливають на нормальний епітелій кон’юнктиви, не уражують секреторні функції келихоподібних клітин, не порушують міжклітинну взаємодію. Завдяки високій адгезії до муцинового компонента слізної плівки та високій в’язкості вони не видаляються з очної поверхні при морганні та не впливають на гостроту зору. Завдяки високій в’язкості при відкритому оці підтримують товщину слізної плівки, а зниження в’язкості при морганні сприяє комфортним відчуттям при закритих очах. При ушкодженнях поверхні ока зменшують сквамозну метаплазію, покращують експресію келихоподібних клітин та морфологію епітеліальних клітин [17].
Використання очних крапель Гілайс® рекомендоване як для покращення комфорту очей при користуванні гаджетами, так і для лікування складних форм синдрому сухого ока. Препарат ефективно підвищує стабільність слізної плівки, забезпечує комфорт поверхні ока та захист від пересихання, формує гладеньку поверхню рогівки і є вибором при носінні контактних лінз. Гілайс® сприяє кращому загоєнню після травм, опіків, операцій та усуває прояви сухого ока.
Список літератури
1. American Academy of Ophthalmology. Dry Eye Syndrome Preferred Practice Pattern. Available from: https://www.aao.org/preferred-practice-pattern/dry-eye-syndrome-ppp-2018 (last accessed 20.04.2021).
2. You I.C., Li Y., Jin R., Ahn M., Choi W., Yoon K.C. Comparison of 0.1%, 0.18%, and 0.3% Hyaluronic Acid Eye Drops in the Treatment of Experimental Dry Eye. J. Ocul. Pharmacol. Ther. 2018. 34(8). 557-564. doi: 10.1089/jop.2018.0032.
3. Troiano P., Monaco G. Effect of hypotonic 0.4% hyaluronic acid drops in dry eye patients: A cross-over study. Cornea. 2008. 27(10). 1126-1130. https://doi.org/10.1097/ICO.0b013e318180e55c.
4. TFOS DEWS II — Tear Film. Available from: https://www.tfosdewsreport.org/report-tear_film/82_36/en/ (last accessed 26.04.2021).
5. Şimşek C., Doğru M., Kojima T., Tsubota K. Current Management and Treatment of Dry Eye Disease. Turk. J. Ophthalmol. 2018. 48(6). 309-313. doi: 10.4274/tjo.69320.
6. Salzillo R., Schiraldi C., Corsuto L., D’Agostino A., Filosa R., De Rosa M., La Gatta A. Optimization of hyaluronan-based eye drop formulations. Carbohydr. Polym. 2016. 153. 275-283. doi: 10.1016/j. carbpol.2016.07.106.
7. Necas J., Bartosikova L., Brauner P., Kolar J. Hyaluronic acid (hyaluronan): a review. Veterinarni Medicina. 2008. 53(8). 397-411.
8. Müller-Lierheim Wolfgang G.K. Why Chain Length of Hyaluronan in Eye Drops Matters. Diagnostics. 2020. 10. 511. doi: 10.3390/diagnostics10080511.
9. Cowman M., Schmidt T., Raghavan P., Stecco A. Viscoelastic Properties of Hyaluronan in Physiological Conditions. F1000Research. 2015. 4. 622. DOІ: 10.12688/f1000research.6885.1.
10. Bothner H., Wik O. Rheology of Hyaluronate. Acta Oto-Laryngologica. 1987. 104. 25-30.
11. Johnson M., Murphy P., Boulton M. Effectiveness of so dium hyaluronate eyedrops in the treatment of dry eye. Graefe’s Archive for Clinical and Experimental Ophthalmology. 244(1). 109-12. DOI: 10.1007/s00417-005-0028-1.
12. Park Y., Song J.S., Choi C.Y., Yoon K.C., Lee H.K., Kim H.S. A Randomized Multicenter Study Comparing 0.1%, 0.15%, and 0.3% Sodium Hyaluronate with 0.05% Cyclosporine in the Treatment of Dry Eye. Journal of Ocular Pharmacology and Therapeutics. 2017. 33(2). 66-72. http://doi.org/10.1089/jop.2016.0086.
13. Yang Y.J., Lee W.Y., Kim Y.J., Hong Y.P. A Meta-Analysis of the Efficacy of Hyaluronic Acid Eye Drops for the Treatment of Dry Eye Syndrome. Int. J. Environ Res. Public Health. 2021. 18(5). 2383. doi: 10.3390/ijerph18052383.
14. Deepon Kar. How Hyaluronic Acid Eyedrops Fit into Dry Eye Treatment. Available from: https://eyesoneyecare.com/resources/how-hyaluronic-acid-eyedrops-fit-dry-eye-treatment/ (last accessed 29.04.2021).
15. Kojima T., Nagata T., Kudo H., Müller-Lierheim W.G.K., van Setten G.-B., Dogru M., Tsubota K. The Effects of High Molecular Weight Hyaluronic Acid Eye Drop Application in Environmental Dry Eye Stress Model Mice. Int. J. Mol. Sci. 2020. 21. 3516. https:// doi.org/10.3390/ijms21103516.
16. Ocular lubricant choice in the treatment of dysfunctional tear syndrome (tear deficiency). Available from: http://www.bucksformulary.nhs.uk/docs/Guideline_371FM.pdf (last accessed 29.04.2021).
17. Aragona P., Giannaccare G., Mencucci R., et al. Modern approach to the treatment of dry eye, a complex multifactorial disease: a P.I.C.A.S.S.O. board review. British Journal of Ophthalmology. 2021. 1(05). 446-453. doi: 10.1136/bjophthalmol-2019-315747.





