
Резюме. Актуальність. Нейроішемічна форма діабетичної стопи (ДС) характеризується поєднаним ураженням периферичних судин і нервів, що призводить до хронічних виразок, больового синдрому та високого ризику ампутацій. Пошук додаткових методів поліпшення периферичної перфузії є актуальним. Цилостазол — інгібітор фосфодіестерази III з вазодилатуючими й антиагрегантними властивостями — потенційно здатний поліпшувати мікроциркуляцію та перебіг нейропатії при цукровому діабеті (ЦД). Цель: оценить клиническую эффективность добавления цилостазола к стандартной терапии у пациентов с нейроишемической формой диабетической стопы, в частности влияние на болевой синдром, частоту ампутаций и риск желудочно-кишечных кровотечений. Матеріали та методи. Проведено відкрите рандомізоване дослідження за участю 72 пацієнтів із цукровим діабетом 2-го типу (ЦД2) та нейроішемічною формою ДС. Дослідна група (n = 38) додатково до стандартної антитромбоцитарної терапії отримувала цилостазол 100 мг/добу, контрольна група (n = 34) — лише стандартну терапію (ацетилсаліцилова кислота в поєднанні з клопідогрелем). Тривалість лікування — 6 місяців. Оцінювали інтенсивність больового синдрому за візуальною аналоговою шкалою (ВАШ), частоту малих та великих ампутацій нижніх кінцівок, випадки шлунково-кишкових кровотеч. Результати. Додавання цилостазолу сприяло суттєвому полегшенню болю: вже через 2 місяці у 84,2 % пацієнтів основної групи інтенсивність болю зменшилася до ≤ 3 бали за ВАШ без потреби в додаткових аналгетиках, тоді як у контролі — лише у 11,76 % (p < 0,001). За 6 місяців частка пацієнтів, яким виконано малі ампутації, була значно нижчою у групі цилостазолу (7,89 проти 32,35 %, p = 0,018). Частота великих ампутацій не відрізнялася (приблизно 5 % в обох групах). Випадки шлунково-кишкових кровотеч були поодинокими (5,26 проти 5,88 %, p > 0,05). Значущих побічних ефектів терапії цилостазолом не виявлено. Выводы. У пациентов с нейроишемической формой диабетической стопы добавление цилостазола к стандартной терапии достоверно уменьшает хроническую боль и потребность в малых ампутациях, не повышая риск желудочно-кишечных кровотечений. Цилостазол можно рассматривать как эффективный и относительно безопасный препарат в комплексном лечении диабетической стопы.
Ключевые слова: диабетическая стопа; микроциркуляция; ангиопротектор; антиагрегантная терапия; сахарный диабет; нейроишемия; ампутация; боль; Плестазол
Введение
Сахарный диабет 2-го типа (СД2) является одной из основных причин развития тяжелых микро- и макрососудистых осложнений. Одно из самых тяжелых осложнений — диабетическая стопа (ДС), которая определяется как поражение стопы у пациента с имеющимся или ранее диагностированным сахарным диабетом, включающее один или несколько из следующих факторов: периферическая нейропатия, заболевание периферических артерий, инфекция, язва (язвы), нейроостеоартропатия, гангрена или ампутация [1, 2]. ДС часто приводит к инвалидизации, снижению качества жизни и существенному повышению стоимости лечения [3]. По оценкам ученых, до 34 % пациентов с СД в течение жизни имеют язвы стопы, а каждые 20 секунд в мире происходит ампутация нижней конечности у больного СД [3].
В последние годы появляются данные о перспективности использования цилостазола — ингибитора фосфодиэстеразы III с вазодилатирующими и антиагрегантными свойствами — в лечении ДС. Сначала цилостазол зарекомендовал себя как эффективное средство для облегчения симптомов перемежающейся хромоты, увеличения безболезненной дистанции ходьбы и улучшения периферического кровотока у больных облитерирующим атеросклерозом сосудов нижних конечностей [4, 5]. Однако дополнительно были выявлены его потенциальные ангиопротекторные и нейропротекторные эффекты у пациентов с СД. В частности, Kim и соавт. (2021) показали, что цилостазол способствует восстановлению эндотелиальной функции в условиях гипергликемии через активацию сигнального пути AdipoR1/SIRT1/AMPK, который играет ключевую роль в поддержании микроциркуляции [3]. Это подтверждает данные исследований, в которых цилостазол предотвратил прогрессирование дисфункции эндотелия и стимулировал ангиогенез в условиях высокой гликемии [6, 7, 10]. Исследование Tsai и соавт. (2022) показало, что у пациентов с заболеванием периферических артерий добавление цилостазола к стандартной антитромботической терапии ассоциируется со снижением риска ампутаций конечности [12].
Клинические рекомендации все больше обращают внимание на цилостазол как составную часть лечения заболеваний периферических артерий. Согласно рекомендациям Европейского общества сосудистой хирургии (ESVS), цилостазол может рассматриваться как эффективный препарат для увеличения дистанции ходьбы у пациентов с перемежающейся хромотой, которым не показано хирургическое вмешательство [15]. Американская ассоциация сердца/Американский колледж кардиологии (AHA/ACC) также присваивает цилостазолу класс рекомендации I для облегчения симптомов у больных перемежающейся хромотой (при отсутствии противопоказаний) [10]. В рекомендациях Международной рабочей группы по диабетической стопе (IWGDF) упоминается потенциальная польза включения цилостазола в мультимодальную терапию пациентов с критической ишемией нижних конечностей при СД [2]. Следовательно, исследование влияния цилостазола на клинические результаты у больных с нейроишемической формой ДС является актуальным и перспективным направлением, которое может открыть новые возможности для уменьшения осложнений и улучшения качества жизни пациентов.
Цель: оценить клиническую эффективность добавления цилостазола к стандартной терапии у пациентов с нейроишемической формой диабетической стопы, в частности влияние на болевой синдром, частоту ампутаций и риск желудочно-кишечных кровотечений.
Материалы и методы
В исследовании приняли участие 72 пациента с СД2, осложненным нейроишемической формой ДС. Критерии включения: возраст 40–75 лет; подтвержденный СД2; наличие периферической диабетической нейропатии с нарушением всех видов чувствительности в стопе и болевым синдромом; хроническая артериальная недостаточность нижних конечностей II–III степени по Фонтейну. Пациенты были рандомизированы на две группы: исследовательскую (n = 38) и контрольную (n = 34). Обе группы не отличались по возрасту, полу, длительности СД, сопутствующим заболеваниям и уровню гликированного гемоглобина (HbA1c), который составлял в среднем 7,4 ± 0,3 %. Контрольная группа получала стандартную двойную антиагрегантную терапию: ацетилсалициловую кислоту 100 мг/сутки и клопидогрель 75 мг/сутки. Исследовательская группа дополнительно получала цилостазол (в нашем исследовании препарат Плестазол производства АО «Киевский витаминный завод») в дозе 50 мг два раза в сутки. С целью профилактики желудочно-кишечных осложнений все пациенты обеих групп получали пантопразол 40 мг/сутки. Все пациенты также получали рекомендации по модификации образа жизни, в частности ежедневных пеших прогулок в удобной обуви продолжительностью 45 минут. Продолжительность наблюдения составляла 6 месяцев с ежемесячным клиническим осмотром. Оценивали динамику болевого синдрома в нижних конечностях по 10-балльной визуальной аналоговой шкале (ВАШ), потребность в дополнительных анальгетиках, частоту выполнения больших и малых ампутаций нижних конечностей, а также случаи желудочно-кишечных кровотечений (ЖКК). Большой считали ампутацию на уровне голени или выше, малой — ампутацию дистальнее голеностопного сустава (пальцы, передняя или средняя часть стопы) [11]. Для оценки достоверности различий частоты событий между группами применяли критерий χ² (с расчетом точного p), а для количественных показателей — t-критерий Стьюдента; значение p < 0,05 считали статистически значимым.
Результаты
В начале исследования все пациенты жаловались на хроническую боль в стопах и голенях, интенсивность которой по ВАШ составляла в среднем 5 ± 1 балл. Через 1 месяц терапии в экспериментальной группе 23 из 38 пациентов (60,25 %) отметили уменьшение боли на 2–3 балла без необходимости дополнительных анальгетиков, тогда как в контрольной группе ни один пациент не почувствовал облегчения без обезболивающих. К концу второго месяца наблюдения доля пациентов с уменьшением боли до 1–3 баллов в экспериментальной группе выросла до 84,2 % (32 из 38), тогда как в контрольной группе только 4 из 34 пациентов (11,76 %) достигли такого улучшения (p < 0,001). В дальнейшем эти показатели оставались стабильными до конца шестого месяца наблюдения: боль была значительно облегчена у большинства (84,2 %) пациентов, получавших цилостазол, в отличие от только 11,76 % пациентов контрольной группы, у которых наблюдалось улучшение (рис. 1). В контрольной группе для облегчения симптомов большинство больных нуждалось в периодическом приеме анальгетиков, тогда как в группе цилостазола дополнительные анальгетики практически не применялись.
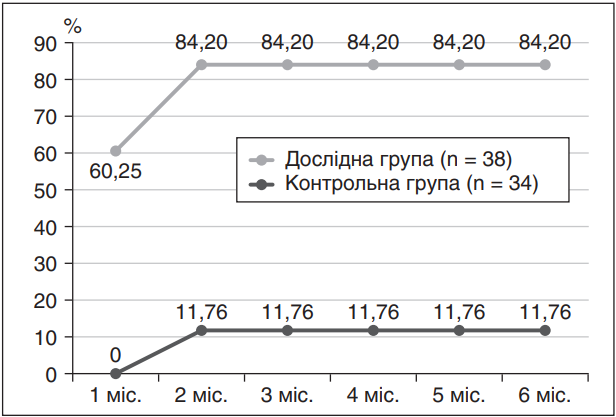
На рис. 1 показано, что со второго месяца терапии цилостазолом доля пациентов с облегчением боли стабильно выше в исследовательской группе, чем в контрольной (разница статистически значима, p < 0,001).
За период наблюдения потребность в крупных ампутациях была невысокой в обеих группах. В целом за 6 месяцев наблюдения частота крупных ампутаций составила 2 случая (5,26 %) в экспериментальной группе и 2 (5,88 %) в контрольной (разница незначительная). В то же время в отношении малых ампутаций (ампутации пальцев или части стопы) различия между группами были существенными. В первый месяц в контрольной и экспериментальной группе выполнено по 2 ампутации. Но на 2–3-м месяце количество новых малых ампутаций в группе цилостазола уменьшилось до нуля, тогда как в контрольной продолжали проводиться оперативные вмешательства по поводу некректомий на уровне пальцев и переднего отдела стопы. В итоге суммарная частота малых ампутаций за весь период составила лишь 3 случая (7,89 % от количества пациентов) в исследовательской группе против 11 случаев (32,35 %) в контрольной группе; эта разница является статистически достоверной (p = 0,018). На рис. 2 сопоставлена частота малых и больших ампутаций в двух группах: видно, что доля пациентов, нуждавшихся в малых ампутациях, в группе цилостазола значительно ниже, чем в контрольной (р < 0,05), тогда как по большим ампутациям разница несущественна.
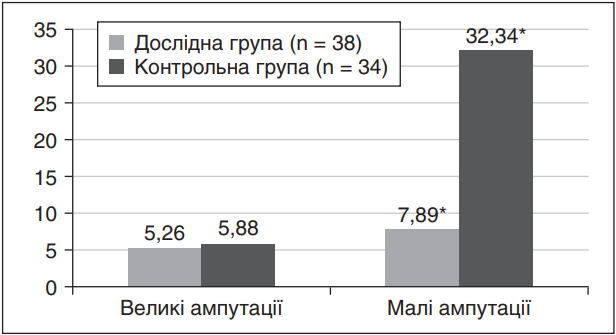
Примечание: * — статистически значимая разница между группами (p < 0,05 для малых ампутаций).
Случаи СКК в течение исследования регистрировались единично и не отличались между группами. В частности, за первые 2 месяца наблюдения было зафиксировано по одному эпизоду нетяжелых СКК в каждой группе (вероятно, гастродуоденальная эрозия на фоне антикоагулянтной терапии), которые успешно лечились консервативно. На 3–4-м месяце отмечено еще по одному эпизоду СКК в разных группах (1 случай в экспериментальной группе на третьем месяце и 1 случай в контрольной группе на четвертом месяце). Таким образом, общая частота ШКК составила 2 случая (5,26 %) в группе цилостазола и 2 случая (5,88 %) в контрольной группе, разница между группами статистически незначима (p > 0,05). Важно, что все эти осложнения имели легкую или среднюю степень тяжести и возникли на фоне нерегулярного приема пациентами ингибитора протонной помпы. Дополнительных серьезных побочных эффектов терапии (таких как головная боль, тахикардия или отеки, характерные для цилостазола) ни в одной группе не отмечено.
В табл. 1 обобщены ключевые клинические результаты в обеих группах за время наблюдения. Как видно, добавление Плестазола наиболее выраженно повлияло на частоту уменьшения болевого синдрома и на снижение потребности в малых ампутациях, тогда как показатели больших ампутаций и ШКК существенно не отличались между группами.
| Показатель | Исследовательская группа (n = 38) |
Контрольная группа (n = 34) |
p |
|---|---|---|---|
| Уменьшение боли (по ВАШ ≤ 3 балла без анальгетиков) | 32 (84,2) | 4 (11,76) | < 0,001 |
| Крупные ампутации | 2 (5,26) | 2 (5,88) | n.s. (p > 0,05) |
| Малые ампутации | 3 (7,89) | 11 (32,35) | 0,018 |
| Желудочно-кишечные кровотечения | 2 (5,26) | 2 (5,88) | n.s. (p > 0,05) |
Примечание: n.s. — различия статистически не значимы.
Обсуждение
Результаты исследования показали, что добавление цилостазола к стандартной терапии пациентов с нейроишемической формой ДС улучшает клиническое течение заболевания. В частности, применение цилостазола привело к достоверному уменьшению интенсивности хронической боли в нижних конечностях. Уже в течение первого месяца 60,25 % больных исследовательской группы отметили облегчение боли без необходимости в анальгетиках, тогда как в контрольной группе такого эффекта не наблюдалось. На втором месяце преимущество цилостазола стало еще более очевидным: боль уменьшилась до легкой (≤ 3 балла по ВАШ) у 84,2 % пациентов, получавших эту терапию, по сравнению с 11,76 % в контрольной группе (p < 0,001). Полученные данные согласуются с известным эффектом цилостазола по облегчению симптомов перемежающейся хромоты и качества жизни пациентов с облитерирующим атеросклерозом сосудов нижних конечностей.
По данным метаанализов, прием цилостазола ассоциируется с повышением максимальной дистанции безболезненной ходьбы на 15 % по сравнению с плацебо. Механизмы этого эффекта связаны как с вазодилатацией и улучшением микроциркуляции, так и с воздействием на эндотелий и метаболические процессы в тканях. В частности, экспериментальные работы подтверждают, что цилостазол активирует сигнальные пути, важные для функции эндотелия (AMPK/SIRT1 и другие), благодаря чему предотвращает эндотелиальную дисфункцию в условиях гипергликемии и способствует неоангиогенезу [7, 16, 18]. Кроме того, некоторые данные указывают, что цилостазол может положительно влиять и на течение диабетической нейропатии. Так, в опытах на животных было показано улучшение регенерации нервных волокон на фоне терапии цилостазолом, вероятно, за счет улучшения кровоснабжения нервной ткани и снижения окислительного стресса [13, 14]. Это особенно актуально для нейроишемической формы ДС, когда сочетаются как сосудистые, так и нейропатические поражения.
Важным клиническим эффектом нашего исследования является значительное снижение частоты малых ампутаций в группе пациентов, получавших цилостазол. За 6 месяцев наблюдения в экспериментальной группе малые ампутации потребовались только 7,89 % пациентов, тогда как в контрольной группе почти треть больных (32,35 %) перенесла оперативные вмешательства на пальцах или части стопы (p = 0,018). Эта разница является клинически значимой, ведь малые ампутации часто предшествуют более масштабным вмешательствам и отражают прогрессирование поражений стопы. Полученные данные согласуются с результатами других исследований. В частности, недавно проведенное многоцентровое исследование в Корее (Cha и соавт., 2023) показало, что у пациентов с СД после эндоваскулярного лечения окклюзий артерий нижних конечностей применение тройной антитромботической терапии (аспирин + клопидогрель + цилостазол) достоверно снижало риск малых ампутаций по сравнению со стандартной двойной терапией (2,0 против 6,3 % за 2 года; HR = 0,35) [8]. В другом метаанализе, включавшем более 3000 пациентов с периферическим атеросклерозом (большинство с критической ишемией конечностей), лечение цилостазолом достоверно улучшало отдаленные результаты реваскуляризации: повышало показатель выживаемости без ампутаций (HR = 0,79) и долю сохраненных конечностей (HR = 0,42), снижало частоту рестенозов и повторных вмешательств [5, 13, 14]. Хотя прямая экстраполяция этих данных на популяцию больных с диабетической стопой требует осторожности, наши результаты подтверждают тенденцию: дополнительная терапия цилостазолом способствует лучшей перфузии тканей нижних конечностей и более быстрому заживлению язвенно-некротических дефектов, что в итоге уменьшает потребность в ампутациях.
Частота крупных ампутаций в нашем исследовании была низкой и не отличалась между группами (по 2 случая в каждой). Это можно объяснить относительно непродолжительным периодом наблюдения (6 месяцев) и тем, что пациентам по возможности своевременно выполняли реваскуляризацию или малые ампутации для профилактики прогрессирования заболевания. Цилостазол не влиял на необходимость крупных ампутаций в такой короткий срок, что согласуется с данными литературы: в упомянутом исследовании Cha и соавт. (2023) частота крупных ампутаций (и повторных реваскуляризаций) была одинаковой между группами с цилостазолом и без него [8]. Однако стоит отметить, что в исследованиях с большей продолжительностью наблюдения дополнительная терапия цилостазолом ассоциировалась с тенденцией к долгосрочному сохранению конечности. Можно предположить, что длительное применение цилостазола в сочетании с полноценным хирургическим лечением способно отсрочить высокие ампутации или предотвратить их у пациентов с критической ишемией.
Безопасность применения цилостазола в условиях комбинированной антитромбоцитарной терапии является еще одним важным аспектом. Известно, что цилостазол как ингибитор агрегации тромбоцитов в целом не повышает риск серьезных кровотечений в той же степени, как антикоагулянты или двойная антитромботическая терапия, поскольку его механизм действия отличается и он обладает также вазопротекторными эффектами [9, 14, 17]. В нашем исследовании частота ШКК в обеих группах была низкой, 5,26 и 5,88 %, разницы между группами не выявлено. Все зафиксированные кровотечения были некритическими (легкой или средней степени тяжести) и возникали преимущественно у пациентов, которые нарушали режим приема ингибиторов протонной помпы. Таким образом, добавление цилостазола не привело к росту ШКК на фоне двойной антитромбоцитарной терапии. Это согласуется с данными об относительно безопасном профиле цилостазола: в исследованиях у кардиологических больных его длительное назначение не сопровождалось повышением риска тяжелых кровотечений по сравнению со стандартной терапией [10]. Типичными побочными эффектами цилостазола являются головная боль, сердцебиение, приливы, понос — они обусловлены вазодилатацией и повышением сердечного выброса. В нашей выборке такие эффекты не наблюдались или были минимальными, что может быть связано с относительно небольшой дозой (100 мг/сутки) и постепенным титрованием препарата.
Учитывая полученные результаты, можно утверждать, что цилостазол является эффективным дополнением к комплексной терапии нейроишемической формы ДС. Особенно целесообразно рассматривать его назначение у пациентов с хронической ишемией нижних конечностей, у которых снижение перфузии сочетается с невропатией и язвенными поражениями и которые уже получают базовую антитромбоцитарную терапию. Наши данные демонстрируют, что добавление цилостазола улучшает симптоматику (боль, хромоту) и может снизить необходимость малых ампутаций, не повышая риска ШКК при условии надлежащей гастропротекции. Это открывает перспективу более широкого применения цилостазола в практике под наблюдением мультидисциплинарной команды (семейного врача, эндокринолога, сосудистого хирурга, кардиолога).
Выводы
1. Добавление цилостазола (в нашем исследовании Плестазол 50 мг 1 р/д) к стандартной антитромбоцитарной терапии у пациентов с нейроишемической формой диабетической стопы достоверно уменьшает интенсивность болевого синдрома по ВАШ уже со второго месяца лечения (р < 0,001).
2. У больных, получавших Плестазол, отмечена значительно более низкая частота малых ампутаций нижних конечностей по сравнению с контрольной группой (7,89 против 32,35 %; р = 0,018), что свидетельствует об улучшении периферической перфузии и репаративных процессов.
3. Частота крупных ампутаций (на уровне голени и выше) в обеих группах была низкой и не отличалась статистически, что, вероятно, связано со своевременным хирургическим вмешательством при прогрессировании заболевания.
4. Случаи желудочно-кишечных кровотечений были единичными (5,26 % — экспериментальная группа, 5,88 % — контрольная группа) и не зависели от наличия цилостазола в схеме лечения; это подтверждает благоприятный профиль безопасности препарата при использовании ингибиторов протонной помпы.
5. Цилостазол можно рекомендовать как эффективный и относительно безопасный компонент комплексной терапии пациентов с нейроишемической формой диабетической стопы. Его применение приводит к облегчению симптомов, улучшает клинический прогноз (снижает риск ампутаций) и не сопровождается значительным повышением частоты осложнений. Дальнейшие исследования с более длительным периодом наблюдения помогут уточнить долгосрочные преимущества дополнительной терапии цилостазолом в этой категории пациентов.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов и собственной финансовой заинтересованности при подготовке данной статьи.
Список литературы
- 1. Armstrong DG, Boulton AJM, Bus SA. Diabetic foot ulcers and their recurrence. New England Journal of Medicine. 2017;376(24):2367-2375. https://doi.org/10.1056/NEJMra1615439.
- 2. International Working Group on the Diabetic Foot. Definitions and criteria for diabetes-related foot disease. 2019. Retrieved from: https://iwgdfguidelines.org.
- 3. Kim MJ, Park KG, Lee KM, Lee MK. Cilostazol improves endothelial function in hyperglycemia via activation of AdipoR1/SIRT1/ AMPK signaling [Abstract 1587]. Diabetes. 2021;70(Suppl 1).
- 4. Tseng SY, Chang HY, Li YH, Chao TH. Effects of cilostazol on angiogenesis in diabetes through adiponectin/AdipoR1/Sirtuin1 signaling pathway. International Journal of Molecular Sciences. 2022;23(23):14839. https://doi.org/10.3390/ijms232314839.
- 5. Cha JJ, Cho JY, Lim S, et al. Effect of cilostazol on patients with diabetes who underwent endovascular treatment for peripheral artery disease. Journal of the American Heart Association. 2023;12(12):e027334. https://doi.org/10.1161/JAHA.122.027334.
- 6. Desai K, Han B, Kuziez L, et al. Literature review and meta-analysis of the efficacy of cilostazol on limb salvage rates after infrainguinal endovascular and open revascularization. Journal of Vascular Surgery. 2021;73(2):711-721.e3. https://doi.org/10.1016/j. jvs.2020.08.125.
- 7. Aboyans V, Ricco JB, Bartelink MEL, et al.; ESC Scientific Document Group. 2017 ESC Guidelines on the diagnosis and treatment of peripheral arterial diseases, in collaboration with the European Society for Vascular Surgery (ESVS). European Heart Journal. 2018;39(9):763-816. https://doi.org/10.1093/eurheartj/ehx095.
- 8. Gerhard-Herman MD, Gornik HL, Barrett C, et al. 2016 AHA/ACC guideline on the management of patients with lower extremity peripheral artery disease: A report of the American Heart Association/American College of Cardiology Task Force on clinical practice guidelines. Circulation. 2017;135(12):e726-e779. https:// doi.org/10.1161/CIR.0000000000000470.
- 9. Hingorani A, LaMuraglia GM, Henke P, et al. The management of diabetic foot: A clinical practice guideline by the Society for Vascular Surgery in collaboration with the American Podiatric Medical Association. Journal of Vascular Surgery. 2016;63(2 Suppl):3S-21S. https://doi.org/10.1016/j.jvs.2015.10.003.
- 10. de Franciscis S, Gallelli L, Battaglia L, et al. Cilostazol prevents foot ulcers in diabetic patients with peripheral vascular disease: A randomized trial. International Wound Journal. 2015;12(3):250- 253. https://doi.org/10.1111/iwj.12085.
- 11. Canonico ME, Piccolo R, Avvedimento M, et al. Antithrombotic therapy in peripheral artery disease: Current evidence and future directions. Journal of Cardiovascular Development and Disease. 2023;10(4):164. https://doi.org/10.3390/jcdd10040164.
- 12. Tseng SY, Chao TH, Li YH, et al. Cilostazol improves high glucose-induced impaired angiogenesis in human endothelial progenitor cells and vascular endothelial cells as well as enhances vasculoangiogenesis in hyperglycemic mice via the AMPK pathway. Journal of Vascular Surgery. 2016;63(4):1051-1062.e3. https://doi.org/10.1016/j. jvs.2014.10.103.
- 13. Musial DC, Ajita ME, Bomfim GHS. Benefits of cilostazol’s effect on vascular and neuropathic complications caused by diabetes. Medical Sciences. 2025;13(1):1. https://doi.org/10.3390/medsci13010001.
- 14. Chiu HW, Shih CC, Huang HJ, et al. Cilostazol attenuates vascular inflammation via the regulation of TICAM1/IRF3 signaling pathway. Biomedicine & Pharmacotherapy. 2025;189:118275.
- 15. Chang L-L, Wu Y-M, Wang H-C, et al. Cilostazol ameliorates motor dysfunction and Schwann cell impairment in streptozotocin-induced diabetic rats. International Journal of Molecular Sciences. 2024;25(14):7847. https://doi.org/10.3390/ijms25147847.
- 16. Petrenko O, Badziukh S, Korsa V, et al. Topical application of autologous plasma-derived plasminogen accelerates healing of chronic foot ulcers in type 2 diabetes patients. The International Journal of Lower Extremity Wounds. 2024. Advance online publication. https:// doi.org/10.1177/15347346241256025.
- 17. Kolosovych IV, Hanol IV. Hemocoagulation factors of hemorrhagic complications in acute pancreatitis. Fiziologichnyi Zhurnal. 2022;68(1):56-61. https://doi.org/10.15407/fz68.01.056.
- 18. Prystupiuk M. The use of inhaled analgesic Umerox (methoxyflurane) in a surgical inpatient setting. PRMD [Internet]. 2025 Jun 17;8(1):15-20. Available from: https://perioperative.org.ua/index. php/prtmdc/article/view/132. Отримано/Received 24.06.2025 Рецензовано/Revised 31.07.2025 Прийнято до друку/Accepted 10.08.2025



 Стаття
Стаття
 Відео
Відео
 Відео
Відео
















